Les conséquences du confinement sont désastreuses et vont nous faire souffrir plusieurs années. Alors que ces deux mois et demi furent délétères pour la France, les limites lourdes à la liberté imposées par le gouvernement empêcheraient-elles la vie de reprendre normalement, tant sur le plan psychique que médical, scolaire, social, économique?
Pourtant nous sommes en fin d’épidémie et les quelques cas encore décelables ne justifient en aucun cas de bloquer 67 millions d’habitants. En revanche, ils justifieraient d’un traitement efficace, utilisé dans le monde entier.
Pourquoi les en priver et en conduire certains à une maladie éventuellement longue sur plusieurs semaines ?
Un but subliminal : poursuivre la terreur ?
Ceci nous conditionnerait à accepter des vaccins (qui ne verront sûrement jamais le jour), ou au moins une drogue chère comme le Remdesivir de Gilead. Il suffit de jeter un rapide coup d’œil aux cours en Bourse de Gilead et de laboratoires tonitruants sur un éventuel vaccin, pour voir que les acrobaties médiatiques du genre Lancet ne sont pas gratuites. Elles permettent, en quelques jours, de doper le cours de l’action boursière et pour les initiés de gagner beaucoup d’argent.
Depuis le desserrement du confinement policier mortifère qui nous a été imposé inutilement, le lobby de la peur essaie d’entretenir la panique créée par les médias et le gouvernement, afin de maintenir notre soumission et l’abandon de notre bien le plus précieux, notre liberté.
En témoignent de nombreux articles mensongers qui prétendent que le confinement aurait « sauvé des vies », qu’il faut « craindre une deuxième vague » d’épidémie parce que « l’immunité collective serait insuffisante » (note 1,2,3), que « l’application stop Covid serait utile ». Même le syndicat des avocats a dénoncé cette application à éviter absolument et à désinstaller, si elle a été installée silencieusement lors d’une mise à jour de votre portable (Note 4).
En réalité, l’épidémie se termine en France comme partout en Europe. Il n’y aura pas de vraie deuxième vague de Covid19, car cela n’est jamais observé dans les maladies virales (Note 5). Et il ne faut pas se préoccuper de la faible prévalence de la maladie dans la population, car l’observation des épidémies précédentes montre que l’immunité collective ne détermine presque jamais leur évolution. L’enthousiasme pour les tests, toujours peu au point, et non spécifiques, ne repose que sur l’envie du gouvernement de perpétuer la peur, et de nous maintenir dans l’angoisse de nouvelles contaminations. Ils n’ont pas d’intérêt alors que l’épidémie est terminée.
Ne cédez pas à la pression des médias et des autorités pour vous faire ficher ; l’usage du test est devenu une arme politique pour faire croire qu’on s’occupe de son peuple, de sa ville. Il n’a plus aucun intérêt à ce stade de disparition de cette virose.
Le confinement aveugle et policier n’a ni diminué, ni ralenti l’épidémie
Contrairement aux prédictions issues des simulations qui l’ont motivé (Note 6), le confinement policier n’a ni ralenti, ni diminué la propagation de l’épidémie. Plutôt que de croire aux annonces de propagande basées sur les succès virtuels de modélisations biaisées (Note 7) qui encensent cette technique moyenâgeuse et inefficace (Note 8), ou de ceux qui veulent à tout prix se consoler d’avoir été emprisonné sans faute, il faut regarder les faits réels, les faits observés, les faits constatés.
Résultats comparatifs des pays confinés ou non, d’après les chiffres OMS
Les données publiées par l’OMS prouvent que la propagation de l’épidémie n’a été ni retardée, ni amoindrie par le confinement aveugle dans aucun des pays qui l’ont imposé à leur population.
Dans les pays confinés, les évolutions du nombre de contaminations quotidiennes avant et après le verrouillage, ne montrent en effet aucun signe de discontinuité (Note 9), ni dans leurs taux de croissance, ni dans leurs temps de doublement. Cette remarque a été le sujet d’un article bien documenté (Note 10). Ceux qui prétendent que le confinement aurait évité l’accélération, protégeant de fait d’une surcharge des hôpitaux, sont démentis par les faits que démontrent les résultats comparés entre pays voisins de même culture.
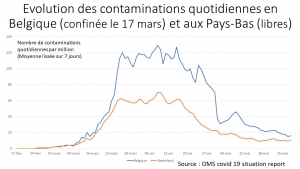
Infections cumulées Belgique versus Pays-Bas
Et si on compare la propagation de l’épidémie dans les pays adeptes du confinement autoritaire à la française à celle observée dans les autres pays, on s’aperçoit que le confinement aveugle a été délétère. A titre d’exemple, la comparaison des courbes d’infections cumulées entre la Belgique (confinée) et les Pays-Bas (non confinés), pays proches, suggère que le confinement policier aurait même pu accélérer l’épidémie. En effet c’est dix à quinze jours après le début du confinement belge que la propagation de l’épidémie s’accélère dans ce pays, alors qu’elle reste stable aux Pays-Bas non confinés.
Le bilan médical actuel du confinement aveugle franco-italien appliqué aussi en Belgique et en Espagne est catastrophique
Pour évaluer la balance avantages/risques du confinement, il ne faut pas se baser sur les résultats des simulations (Note 10) qui inventent des morts virtuels, théoriques, mais se baser uniquement sur les faits réels, avérés et publiés.
Mortalités comparées
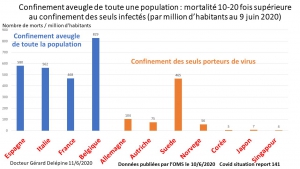
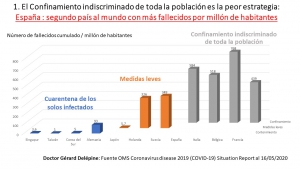
D’après les données publiées par l’OMS le 30 mai 2020 (note 11), la mortalité directe du Covid19 est beaucoup plus élevée dans les pays qui ont pratiqué le confinement aveugle (sans séparer les porteurs de virus des autres) et autoritaire (avec contrôle policier), que dans ceux qui ont pratiqué la quarantaine ciblée (réservée aux seuls porteurs de virus) et fait confiance à leurs citoyens (conseillés et non astreints à domicile).
Au 29 mai 2020, exprimée par million d’habitants, la mortalité officielle directement liée au Covid19 atteint 810 en Belgique, 621 en Espagne, 548 en Italie et 459 en France, pays adeptes du confinement aveugle et policier, contre 100 en Allemagne, 98 au Danemark et 4 à 7 dans les pays asiatiques démocratiques qui n’ont pas confiné leur population.
En adoptant les mesures sanitaires de l’Allemagne, nous aurions probablement 23.000 morts de Covid19, en moins à déplorer. Et sans aucune mesure sanitaire, à l’instar des Pays-Bas, nous pourrions avoir eu 6.100 morts directes du Covid19 en moins.
Morts de Covid19 ou suspectés, et morts « politiques « liées aux conséquences d’une mesure politique et non sanitaire (note 12)
A ce surplus de mortalité directe lié au confinement aveugle, il convient d’ajouter les victimes collatérales et en particulier les malades souffrant de pathologies chroniques (cancéreux, cardiaques, déprimés) qui ont subi l’arrêt des traitements prévus, arrêt imposé par le plan Blanc (note 13) et les nouveaux malades qui n’ont pas pu être diagnostiqués, ni traités du fait de l’interdiction d’opérer les malades non reconnus urgents par les agences régionales de santé.
Les morts pendant le confinement, et les décès anticipés, non dus au Covid19 mais au retard de soins (note 14)
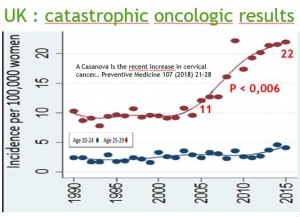
Depuis le début du confinement, 75.000 nouveaux cancers auraient dû être diagnostiqués si les chirurgiens avaient pu opérer. Même l’académie de chirurgie s’en inquiète dans son communiqué du 15 Mai : « depuis la mise en place du Plan Blanc le 13 mars, 85% des 7,2 millions d’interventions chirurgicales programmées chaque année en France ont été reportées, soit près d’1,1million d’actes (CNAMTS, ATIH). Il en résulte des risques d’aggravation dus au retard de prise en charge, non seulement en oncologie, mais également dans les autres disciplines ».
Plus d’un million d’interventions auraient été déprogrammées, remises aux calendes grecques, puisqu’on ne sait toujours pas quand le véritable déconfinement aura lieu, et que les mesures déjà discutables au début de l’épidémie sont maintenant imposées alors qu’elles sont aujourd’hui devenues complètement inutiles.
De combien de morts supplémentaires ces retards aux traitements seront-ils responsables ? Et cette rupture de soins ne concerne pas uniquement la cancérologie, mais a touché toutes les pathologies non Covid, qu’il s’agisse de cardiologie (infarctus dont seulement la moitié des malades attendus se sont présentés en consultation), de neurologie (là aussi moitié moins d’accidents vasculaires constatés à l’hôpital), d’endocrinologie, rhumatologie etc. (note 15)
Alors que l’épidémie se termine et que les hôpitaux sont aux trois quarts vides, le plan blanc a interdit jusque récemment aux chirurgiens d’opérer (note 16), blocage maintenu par les agences régionales de santé pour une durée indéterminée et un nombre croissant de victimes supplémentaires. (note 17). L’étau semble se desserrer, mais les cliniques craignent de manquer de produits anesthésiques, alors que les besoins en réanimation sont en grande baisse.
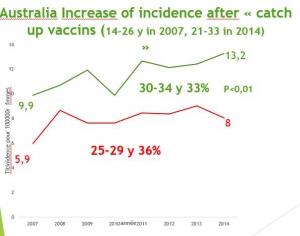
Le bilan médical du confinement devra aussi prendre en compte les complications psychologiques et en particulier les suicides liés à l’astreinte à domicile, aux pertes de salaires et au chômage que constate déjà la presse australienne (note 18, 19 20)et qui pourrait atteindre jusqu’à 150000 victimes aux USA si le déconfinement est trop lent (note 21). Ce bilan n’est pas près d’être terminé.
Les raisons du dramatique échec médical du confinement à la française
Les simulations des prophètes de l’OMS qui ont convaincu de nombreux gouvernements de confiner aveuglément leurs populations ont très largement surestimé le risque réel de la maladie virale et oublié les autres pathologies, le gain espéré de leur mesure et refusé de prendre en compte les complications médicales, sociétales et économiques qui s’annoncent catastrophiques. Nos gouvernants, plutôt que de croire ces prophètes de malheur auraient dû suivre l’exemple des pays asiatiques démocratiques qui ont protégé leurs populations du covid19 et des complications du confinement policier aveugle à la française.
Dans toute l’histoire de l’humanité la lutte contre les épidémies repose sur l’hygiène, la compréhension des modes de propagation des maladies infectieuses, la mise en place de mesures efficaces de désinfection et la séparation des porteurs de germes de la population saine. Ainsi, actuellement le règlement sanitaire international prévoit en cas de peste, l’isolement de tout le groupe de voyageurs, même si une seule personne est touchée, tandis qu’en cas de fièvre jaune ou de choléra, seul l’isolement de la personne atteinte est obligatoire.
Le confinement aveugle de toute une population tel qu’il nous a été imposé est une mesure connue pour être inefficace. En France, elle avait été utilisée pour la dernière fois lors de la peste de Marseille entraînant la mort de la moitié de la population de la ville, sans empêcher la diffusion de la maladie à toute la Provence avec 70.000 victimes supplémentaires. Cette méthode du passé, remise à la mode par la dictature chinoise, a été présentée par le mathématicien -prophète de l’OMS, N Ferguson comme la méthode la plus efficace (note 23 24) de lutte contre l’épidémie.
Mais la simulation de l’Imperial College n’avait apparemment pas envisagé que le confinement d’un adulte malade à la maison (avec seulement du doliprane) constituait le meilleur moyen de contaminer toute la famille, voire les voisins.
Un confinement aveugle sans réflexion
Il eut fallu réfléchir à l’illogisme d’enfermer soignants, policiers ou agents de transport RATP, bus, etc. exposés à de fortes charges virales qui vont et viennent avec leurs familles bloquées à domicile, en milieu clos peu aéré (en raison de la peur transmise sur les médias du vol de virus à travers l’air extérieur, « au-dessus d’un nid de coucous »).
Même si les autorités n’y avaient pas pensé, rien ne les empêchait de rajuster la mise lorsqu’il apparut au début de l’épidémie et la virulence du coronavirus que les soignants étaient les plus rapidement et fortement touchés. D’ailleurs soulignons que les autorités nous ont vanté, tout au long de cet enfermement liberticide accompagné de mesures humiliantes, le modèle de Wuhan. Mais les Chinois, eux, recherchaient avec opiniâtreté les citoyens fiévreux dans les appartements et extrayaient les personnes suspectes pour les isoler rapidement de leur famille.
Nous n’avons retenu que l’autoritarisme chinois, mais moins la logique sanitaire.
Incompétence ou malveillance des ARS ?
Les directions des Agences Régionales de Santé ont imposé aux responsables d’EHPAD de garder les infectés de retour des urgences, y compris après un séjour à l’hôpital où ils avaient été étiquetés Covid19. Ils revinrent sans traitement autre que le doliprane et donc rien ne permettant de faire baisser la charge virale. Ils rejoignirent les autres résidents au moins dans les premières semaines et personne ne s’étonna de la forte contamination chez les ainés, de plus fragiles. N’auraient-ils pas dû comprendre qu’ils favorisaient ainsi la contamination de tous les pensionnaires pourtant les plus fragiles d’entre nous, ceux qu’ils devaient protéger ?
Au-delà du 20 Mars et la circulaire précédent le décret Rivotril du 26 mars (note 24) interdisant le traitement actif des ainés et autorisant l’injection de Rivotril en cas d’insuffisance respiratoire possiblement Covid, les patients ne furent même plus envoyés aux urgences pour préciser le diagnostic. Les habituels infarctus, embolies pulmonaires ou pneumonie bactérienne furent laissés de côté et le résident atteint bientôt euthanasié et étiqueté Covid19.
Que penser du ministre dont les décrets ont interdit la chloroquine soi-disant dangereuse pour prôner le Rivotril à coup sûr mortel en cas de complications respiratoires !
Curieusement, les simulations n’imaginèrent pas non plus que les soignants (qui ne disposaient pourtant pas de protection lors du premier mois de l’épidémie) puissent contaminer leurs malades venus consulter ou leurs voisins dans les transports publics.
Ni que les employés des transports publics et les policiers puissent être contaminés et contaminants parce que non protégés (même interdits de l’être par leur ministre). On entendit ainsi un haut responsable de la santé déclaré à la télévision que les soignants malades s’étaient infectés chez eux !
La sommation de ces erreurs explique que les pays adeptes du confinement strict, mais sans isolement des malades ou des personnes à risque, comme les soignants, comptent davantage de morts que ceux qui ont pratiqué les méthodes médicales éprouvées de l’endiguement (quarantaine) et même que ceux qui n’ont presque rien imposé à leurs populations (Pays-Bas, Suède, Islande).
Le rôle et la responsabilité de l’OMS, ainsi que de Neil Ferguson de l’Imperial College seront à évoquer en détail lors d’une enquête sur le devenir et l’efficacité de nos contributions à cette organisation ainsi qu’à ses publications. La confiance n’excluant pas le contrôle, il sera d’autant plus important de conduire un audit approfondi des recommandations faites par l’OMS qui a ce jour donne plus le sentiment de se comporter comme la FIFA jadis. Verra-t-on le prochain scandale venir des modes opératoires de l’OMS ? FIFA gate, OMS gate ?
Il faudra aussi auditer les décisions publiques autoritaires qui ont été prises en France ont été particulièrement nocives et justifient des enquêtes approfondies (note 25) pour éviter que cela ne puisse se reproduire. Un regard sur la politique italienne de réduction de la mortalité journalière est parlant.
Heureusement, l’épidémie se termine en France comme dans les autres pays d’Europe
Les données publiées par l’OMS montrent que l’épidémie se termine en Europe continentale et en Méditerranée orientale. Depuis la seconde semaine d’avril, le nombre moyen quotidien de nouvelles contaminations a régulièrement diminué ; ce recul atteint 92% en France et dépasse les 85% chez la plupart de nos voisins, même ceux qui présentaient les plus gros chiffres de contaminations depuis le confinement.
La comparaison de l’évolution de l’épidémie en Belgique et aux Pays-Bas, proches par leur situation géographique et leurs modes de vie, est particulièrement frappante et questionne une fois de plus sur l’utilité même du confinement. En effet, les Pays-Bas, qui n’ont pas restreint les libertés publiques, bénéficient de la même régression (83%) de l’épidémie et dans les mêmes délais que la Belgique confinée policièrement après avoir pleuré au total 344 décès par million d’habitants contre 810/1000000 en Belgique.
Il n’y aura pas de deuxième vague (note 26) ou se sera une vaguelette comme pour les autres épidémies
Lors des épidémies virales il n’existe pratiquement jamais de deuxième vague du même virus. Il y a eu précédemment deux épidémies comparables : le SRAS et le Mers et aucune ne s’est exprimée en plusieurs vagues.
Après quelques mois et sans qu’on ne sache pourquoi, l’épidémie s’éteint même si au total peu de personnes ont été immunisées. Contrairement à ce que prétendent les simulations et en particulier celle de Ferguson ou de ses élèves de l’institut Pasteur parisien, ce n’est pas le pourcentage de personnes immunisées qui explique l’arrêt des contaminations.
Le professeur Jean-François Toussaint, lors d’un entretien à la Charente Libre, précise que l’hypothèse d’une deuxième vague est très peu crédible « sur l’analyse dans les 188 pays qui ont déclaré des cas et sur la dynamique évolutive de la maladie ».
Mais certaines épidémies, comme la grippe dont le virus ne dure le plus souvent qu’une saison, reviennent chaque année.
Et jusqu’ici, nous surmontions ces épreuves sans imposer à la population des mesures autoritaires injustifiées et souvent ubuesques qui ont aggravé la situation sanitaire immédiate et impacté l’économie pour plusieurs années.
Le tsunami économique qui nous attend sera pire que celui de 1930
Selon l’Observatoire Français des Conjonctures Economiques (Note 27), les huit semaines de confinement ont déjà diminué le PIB 2020 de 120 milliards d’euros (soit 5 points de PIB). Les secteurs les plus durement touchés sont ceux des transports, de l’hébergement et de la restauration, la construction et les activités de loisirs et le commerce de détail. En tenant compte du rétablissement ralenti par la persistance incongrue des mesures de déconfinement, l’impact global pour 2020 serait de -10 points de PIB.
D’après l’INSEE, le PIB français diminuerait d’environ 20 % au deuxième trimestre 2020 (après –5,8 % au premier). Ce serait la plus forte récession depuis la création des comptes nationaux français en 1948. Même si l’activité économique revenait intégralement à son niveau d’avant crise dès le mois de juillet, le PIB français diminuerait de 8 % sur l’année 2020, or un retour aussi rapide à la normale semble peu réaliste. L’impact global de la crise sanitaire en 2020 sera donc certainement supérieur à ce chiffre.
L’Organisation Internationale du Travail alerte sur les ravages sanitaires et sociaux de la crise qualifiant l’impact sur l’emploi de profond, d’une grande portée et sans équivalent. 1,25 milliard de travailleurs sont exposés à des licenciements, pertes d’activité et de revenus, du fait du confinement dans le monde.
Comme toutes les grandes crises économiques, celle de 2020 a été baptisée : celle du « Grand Confinement » par Gita Gopinath. Selon les prédictions du FMI, l’économie mondiale va connaître « sa pire récession depuis la Grande Dépression ».
Et lorsqu’on constate que l’étendue (5 817 385 infectés) et la mortalité mondiale (362 705) du Covid19 au 30 mai, se situent dans la fourchette basse des grippes saisonnières (environ 20 millions d’infectés et 290 000 à 550 000 morts), on peut déplorer que les mesures injustifiées pour lutter contre une fausse pandémie aient créé une vraie misère.
En urgence, lever les mesures liberticides inutiles et toxiques
Ces constatations conduisent à demander en urgence aux décideurs de lever les mesures coercitives de confinement encore imposées :
Reprendre les activités scolaires partout, à tous les âges et sans mesure de distanciation ni masques, particulièrement chez les petits très traumatisés par ce théâtre tragique.
Libérer les « EHPAD » dans lesquels nos ainés sont devenus des bêtes de zoo, dans leurs prisons même pas dorées. (Note 28) Signez les pétitions pour accélérer leurs sorties de prison, alors que leur seule faute est le grand âge et/ou la dépendance.
Libérez l’activité économique, dans les cafés, restaurants etc. Ces mesures de distanciation imposées sont grotesques, alors que l’épidémie se termine et bloquent de fait la reprise économique dont le pays a tellement besoin.
Impérativement rendre aux médecins de ville et d’hôpital leur liberté de soigner, en particulier libérer la prescription de chloroquine après le triste feuilleton de l’étude biaisée ou inventée du Lancet et la décision brutale du ministre d’aggraver encore le décret mortifère du 26 Mars.
Abroger les décrets liberticides du 26 mars et sa prolongation injustifiée.
Faire stopper complètement le plan blanc, afin que les chirurgiens puissent reprogrammer leurs patients, les rassurer et finalement les soigner. Le bilan spécifique du plan blanc devra être passé à la loupe, car complètement inutile et extrêmement toxique pour les patients et leurs équipes chirurgicales.
Selon Frédéric Bizard, « l’impact sur le volume de la crise Covid19 a été estimé en chirurgie avec une baisse comprise entre 1,7 million et 2 millions d’actes chirurgicaux, soit une chute du volume comprise entre 25% et 29% selon la date de levée du plan blanc. L’évolution des tarifs a été estimée selon les engagements gouvernementaux de 2019 pour les années 2020 à 2022 en chirurgie. L’impact économique global est compris entre 4,2 milliards d’euros et 5 milliards d’euros de baisse des dépenses de chirurgie pour l’assurance maladie en 2020 ». (Note 29)
Activités médicales interdites pour RIEN ! Tout Covid, rien que Covid
Les lits libérés restèrent vides tant en privé qu’en public, et la surcharge en réanimation jamais soulagée par cette privation générale d’activité, les ARS, encore elles, ayant refusé de transférer les malades dans les lits privés (sauf en IDF dans quelques établissements), préférant jouer à la guéguerre à coups d’hélicoptères, et de TGV avec transferts en France ou à l’étranger. En public, ce fut la même chanson, pas d’autres malades que covid19 sauf urgence extrême. Les internes se sont beaucoup ennuyés pendant deux mois et racontent avec beaucoup d’émotion les pertes de chance de leurs patients « habituels ».
Quant au Ségur (Note 30), il est certain que si l’on en espère quelque chose, il serait impératif qu’il se déroule avec une équipe neuve, sous la houlette d’un ministre non responsable des erreurs récentes avant et pendant la crise sanitaire, et surtout après la prise de position ahurissante du ministre de la santé interdisant la chloroquine sur la foi d’un article complètement caviardé, qu’il ne peut avoir lu, et qui fait de nous la risée du monde entier.
Bien curieux film que la gestion de ce Covid19 qu’aucun scénariste n’aurait osé écrire. Pas crédible !
de nombreux commentaires méritent lecture : par exemple en copie sur le site Les 7 du Québec
« En résumé, il y a eu sur-réactions en chaîne, en sacrifiant l’activité du pays au risque … épidémique.
A noter, le mutisme absolu de l’opposition.
1° – La crainte d’une épidémie ?
Non, même si les architectes de l’ordre mondial et leurs partisans l’ont possiblement lorgnée.
2° – Sur-réactions des autorités ?
Non plus, hors divagations significatives…
– 13 janvier 2020 – En l’absence de données scientifiques sur le sujet (!), Jérome Salomon, directeur général de la santé, par délégation pour Agnès Buzyn (dont l’incompétence fût patente et dangereuse), classe de facto l’hydroxychloroquine « sur la liste II des substances vénéneuses ».
19 février 2020 – Macron a décidé de manifester sa solidarité avec le peuple chinois confronté au coronavirus, et annonce l’envoi de 17 tonnes de matériels médicaux (masques, gants, produits désinfectants, combinaisons médicales de protections) à destination de Wuhan. Avec, entre autres, l’appui du groupe LVMH selon France Diplomatie.
– 26 février 2020 – autorisation du match de football O.L/Juventus, au Groupama Stadium à Décines (15 km de Lyon).
Avant de rejoindre le stade, une dizaine de milliers de supporters turinois (bien plus que les 3 000 attendus) se sont baladés toute l’après-midi dans les rues de Lyon, à un moment où la Lombardie, notamment, était déjà particulièrement affectée par le coronavirus.
– 6 mars 2020 – Sortie médiatisée de Macron et Brigitte au théâtre Antoine à Paris.
La pièce « Par le bout du nez » met en scène un tout nouveau président qui, pris d’une démangeaison nasale alors qu’il doit prononcer son discours d’investiture, est contraint de consulter un psychiatre.
Voilà qui laisse songeur …
Selon des témoins, Macron aurait alors déclaré : « La vie continue. Il n’y a aucune raison, mis à part pour les populations fragilisées, de modifier nos habitudes de sortie ».
11 mars 2020 – Tweet Emmanuel Macron @EmmanuelMacron :
« Nous ne renoncerons à rien.
Surtout pas à rire, à chanter, à penser, à aimer. Surtout pas aux terrasses, aux salles de concert, aux fêtes de soir d’été… ».
Cocaïné le président … ?
– 15 mars 2020 – 1er tour des municipales.
Macron, Levy, Buzyn, Philippe et tant d’autres savaient, et auraient choisi de se taire ?
– 15 mars 2020 – Après être allée voter, sortie médiatisée de Brigitte Macron sur les quais de Seine à Paris. Masquée et accompagnée de ses gardes du corps, elle saluait les badauds en leur demandant de « rester à distance respectable ».
La mise en scène n’a pas de secrets pour une ancienne prof de théâtre.
– 17 mars 2020/12:00 – ordre de confinement généralisé de la population.
Aucun problème pour d’éventuelles suites ou poursuites. Dans un grand élan de solidarité parlementaire, les apôtres du confinement se sont auto immunisés … contre la justice.
On ne peut donc que noter l’absence de risque épidémique.
3° – Vent de panique ?
Non. Sauf réactions politiques inappropriées, l’inavouable étant de justifier l’effondrement de l’économie par le confinement, lequel effondrement – épidémie ou pas – se serait de toute façon matérialisé suite à la gestion vereuse et calamiteuse du pays depuis des dizaines d’années.
Miracle, c’est la faute au coronavirus ! Il arrive à point nommé celui-là.
– 21 mars 2020 – Sur LCI, le professeur Christian Perronne (PU-PH) alerte sur la disparition totale des stocks d’hydroxychloroquine en France.
21 mars 2020 – Mise en scène sur mesure pour E. Macron. Montage d’une structure hospitalière (militaire) de campagne à Mulhouse. Capacité initiale « 30 lits réanimation » aussitôt passée à 20 lits.
Opérationnelle le 24 mars 2020, en partie démontée dès le 17 avril 2020, matériels/lits/respirateurs retirés le 22 avril 2020.
Sans parler du coût d’une telle prestation, de qui se fiche-t-on ?
– 22 mars 2020 – Communication navrante et inopportune d’Ursula von der Leyen, présidente de l’UE, via une vidéo à destination des peuples européens, où elle se met en scène dans une séquence de lavage des mains.
« Inopportune » dans la mesure où l’UE a été la grande absente dans cette crise dite « sanitaire ».
L’infantilisation dans la communication n’est pas de bonne augure.
– 27 mars 2020 – Les médecins généralistes ne sont plus autorisés à prescrire l’hydroxychloroquine. On se demande bien pourquoi ?
Il apparaît choquant que c’est l’Ordre des Médecins qui est à la manoeuvre alors que cette Institution est responsable des déserts médicaux en France.
La non indépendance du CNO (Conseil National de l’Ordre), et en particulier de son Président, par rapport à certaines « influences » est mise en cause.
– Parallèlement à une tension due au manque d’approvisionnements en Plaquenil (dérivé hydroxychloroquine), les pharmaciens ne peuvent plus vendre ni masques ni tests. Pourquoi ?
Les cliniques privées ne peuvent pas accueillir les malades du civil (3 000 lits sont restés inoccupés). Pourquoi ?
– Les pensionnaires contaminés dans les EHPAD avaient droit au Rivotril, avec le succès qu’on lui connaît.
– 8 avril 2020 – Castaner, ministre de l’Intérieur, affirme devant la Commission du Sénat qu’il n’y a « pas eu de réquisition, ni par l’armée ni par qui que ce soit » des masques commandés par la région Bourgogne-Franche-Comté.
– 10 avril 2020 – Suite à la plainte pour réquisition de masques à l’aéroport de Bâles/mulhouse , Castaner reconnaît les faits. Inutile de poursuivre dans le parjure, les documents confirmant cette « réquisition » commencent à sortir. Mensonge d’Etat avéré, sans conséquence aucune pour son auteur.
– 24 avril 2020 – Suite à la polémique, le Ministère des Armées reconnaît « avoir acheté, par précaution, un stock important de chloroquine … à la Chine ».
Étrange explication, d’autant que cette molécule avait été classée « vénéneuse » en … 1999, ce qui avait entraîné de facto la même issue pour l’hydroxychloroquine en janvier 2020.
– 18 mai 2020 – L’attitude plus que déconcertante de l’OMS dans cette affaire, ses stratégies divergentes, le vaccin « obligatoire » pour tous, sèment le trouble quant aux réelles compétences de ses membres et à l’occulte dépendance de l’Institution aux lobbies pharmaceutiques.
– 26 mai 2020 – La très sérieuse revue médicale « The Lancet » y est allée de sa plume, et a publié – avant de se rétracter le 4 juin suivant – une étude falsifiée dans laquelle le ministre de la santé Olivier Veran a foncé tête baissée pour justifier l’interdiction de l’hydroxychloroquine.
Bien synchronisé ce coup là !
– 2 juin 2020 – Appli Stop Covid19. Tester la population et voir si elle se soumettait aux mesures liberticides imposées.
Demander aux peuples de la rigueur dans la gestion financière, pour mieux relancer l’économie, alors que ces mêmes prophètes étaient, et sont encore aux premières loges pour accélérer la débâcle, est d’un cynisme abyssal.
Nous sommes gouvernés par des imposteurs et le masque est devenu muselière.
Le rideau de fumée commence à piquer les yeux. Ce n’est plus de masques qu’on a besoin, mais de lunettes.
En résumé, il y a bien eu « conspiration ».
Libre à ceux qui veulent croire à la fable de la chauve-souris et du pangolin. »