Refusons la tyrannie pseudo-sanitaire que l’OMS veut nous imposer

16/04/2024 (2024-04-13)
[Publication initiale : profession-gendarme.com]
Par Dr Gérard Delépine
Durant la crise Covid, l’OMS a été l’instigatrice de mesures contraires aux libertés et aux données de la science. Elles se sont révélées inefficaces contre la maladie, extrêmement dommageables pour les populations qui y ont été soumises et source de profits colossaux pour les élites.
Mais l’OMS, institution non démocratique, non élue et financée à plus de 80 % par des groupes d’influence privés, veut recommencer et, pour y parvenir plus facilement, disposer de pouvoirs supranationaux qui lui permettraient d’imposer une dictature mondiale totale au service de Big Pharma, des GAFAM et des milliardaires.

[Voir aussi :
LETTRE OUVERTE À
ORGANISATION MONDIALE DE LA SANTÉ
et :
]
Les dramatiques échecs des recommandations OMS contre le Covid
Les chiffres de l’épidémie de Covid, publiés par l’OMS et mis en courbe par l’université J. Hopkins, montrent qu’aucune des mesures contraignantes de l’OMS (confinements, obligations du port des masques, pass, obligations vaccinales) n’a été efficace contre la maladie. 939 000 scientifiques et médecins de tous les pays du monde l’avaient clairement annoncé par la déclaration du Great Barrington1.
Nous avions, dès le 27 mars 2020, dénoncé l’imposture des confinements aveugles2 3 4 5. La comparaison des données des Pays-Bas (non confinés) et de la Belgique (sévèrement confinée) a depuis illustré leur nocivité tant sur la recrudescence des infections que sur la mortalité. Avant le confinement, le nombre de contaminations journalières et la mortalité par million étaient semblables dans ces deux pays voisins semblables par leurs démographies et leur mode de vie. Le confinement a fait exploser les contaminations puis la mortalité en Belgique, tandis qu’elles augmentaient deux fois moins aux Pays-Bas non confinés.
Nous avions aussi rappelé6 que la littérature internationale7 montrait que le port généralisé du masque ne protège pas des infections virales. Les données OMS l’ont confirmé : lors du pic d’Omicron les français, soumis à l’obligation du masque ont souffert de 50 % de plus de contaminations journalières/million que les Suédois, non masqués (6000/M versus 4000/M).
Les pseudo vaccins recommandés par l’OMS, et présentés par notre ministre de la santé comme très efficaces, ont été incapables de prévenir la transmission de l’épidémie comme chacun a pu l’observer autour de soi et comme le montrent les comparaisons des données OMS entre les pays très vaccinés et les autres :
Et, contrairement à la propagande de l’OMS et des gouvernements occidentaux, les pseudovaccins n’ont pas non plus protégé les populations ni des formes graves, ni de la mort8 9 :
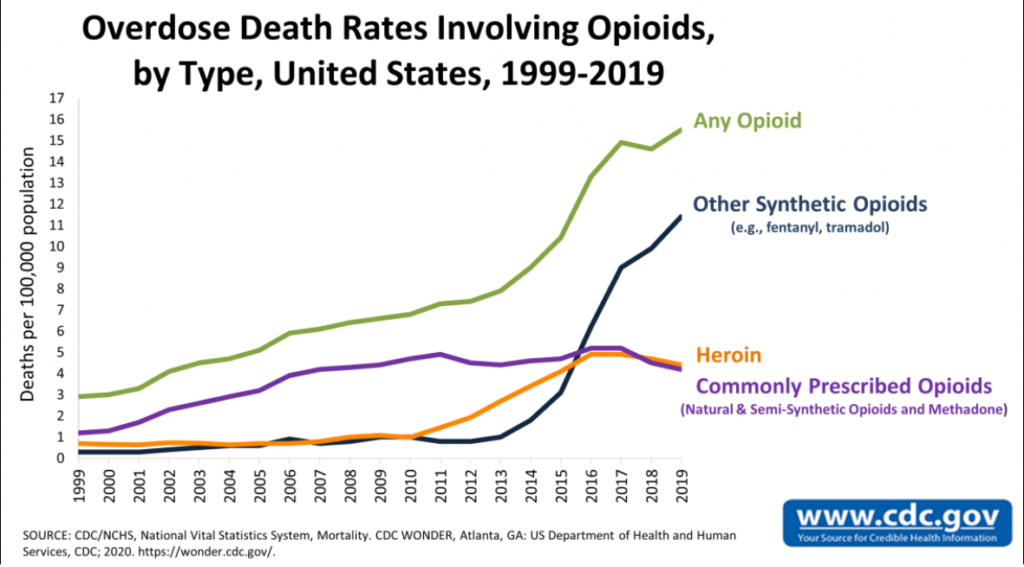
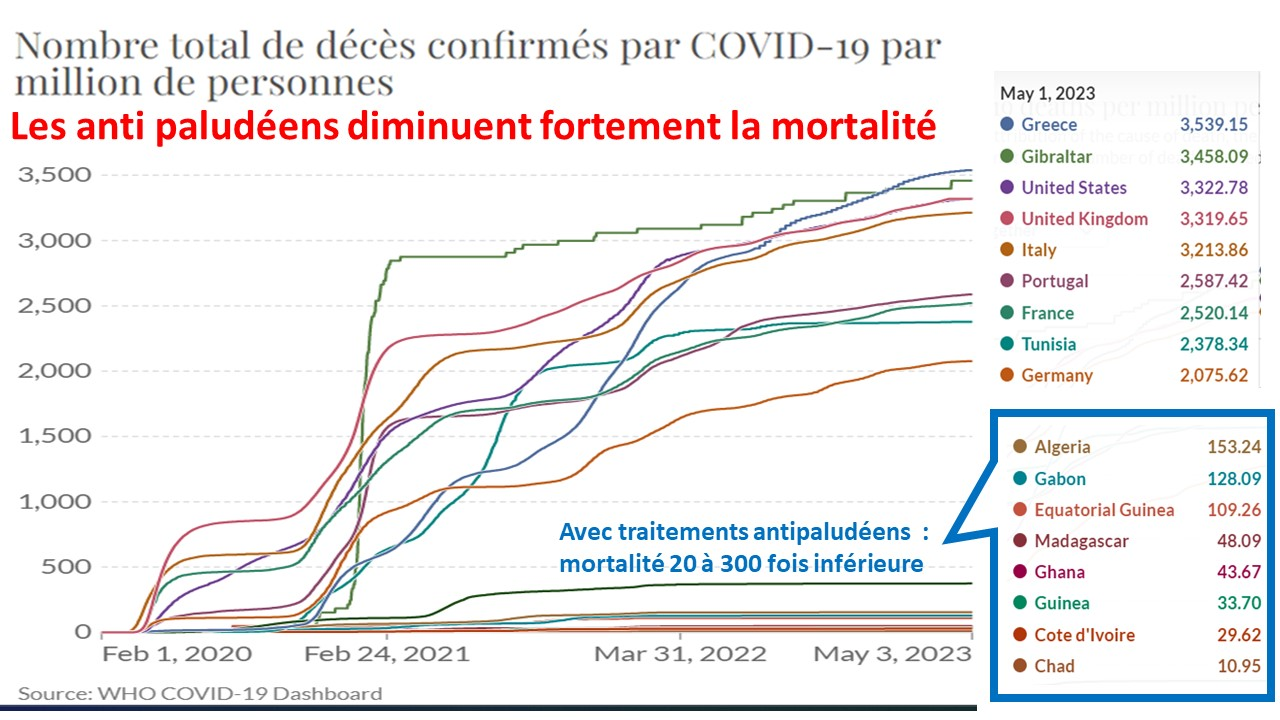
L’OMS a également prétendu que les traitements précoces étaient inefficaces et milité pour leur interdiction, alors que l’usage du traitement Raoult a sauvé les populations des pays qui l’ont utilisé comme la Côte d’Ivoire, le Sénégal ou l’Algérie (ou la proportion de plus de 65 ans est égale à celle de la France)
Totalement inefficaces les recommandations de l’OMS ont été de plus extrêmement dommageables pour les populations qui les ont subies.
Les confinements ont été source de troubles psychologiques graves persistants10 11, de retards scolaires12, de retard de traitements13, de pertes économiques sans précédent14 et d’un endettement colossal15, d’une aggravation mortifère de la famine en Afrique16.
Les masques ont souvent aggravé les infections respiratoires.
Les pseudo vaccins ont été responsables de nombreuses complications en particulier cardiaques (myocardites), neurologiques, de troubles menstruels et de morts subites.
Les mesures Covid de l’OMS ont permis un enrichissement colossal des milliardaires17.
La fortune des milliardaires dans le monde a augmenté en 19 mois de pandémie Covid plus qu’au cours de toute la décennie précédente.
De mars 2020 à octobre 2021, la fortune des milliardaires français a augmenté de 86 %. Les 5 premières fortunes de France ont gagné 173 milliards d’euros et doublé ainsi leur richesse d’avant le début de la pandémie. Ils ont ainsi capté l’équivalent des trois quarts des 240 milliards du « quoi qu’il en coûte »18. Les 5 milliardaires français les plus riches possèdent désormais autant que les 40 % de leurs compatriotes les plus pauvres.
Avec les milliards d’euros engrangés en 19 mois par les milliardaires français, on aurait pu quadrupler le budget de l’hôpital public ou distribuer un chèque de 3500 euros à chaque Français.
La politique de l’OMS est dictée par ses financeurs privés
Lors de sa création par l’ONU en 1948, l’OMS était financée uniquement par les états en fonction de la fortune et de la population de chaque pays. Mais progressivement les principaux états contributeurs, déçus des politiques adoptées, ont diminué leurs contributions tandis que des entités privées (dont des laboratoires pharmaceutiques, Bill Gates et les fondations Gavi et Bill Melinda Gates prenaient le relais.
Lors de l’exercice 2022-2023, seulement 16 % des ressources de l’OMS provenaient des contributions obligatoires des États membres19 tandis que Bill Gates y participait pour près de 40 %, directement ou indirectement, par ses fondations. Bill Gates est devenu le premier financeur de l’OMS et son influence sur les décisions de l’organisme est d’autant plus importante que la majorité de ses contributions sont fléchées, destinées uniquement à un but précis (pour Bill Gates les vaccinations, si possibles obligatoires, pour toutes les maladies, partout et toujours).
German Velasquez, ancien directeur à l’OMS déclarait à l’occasion d’un entretien sur la politique OMS contre le paludisme20 :
« Les acteurs privés, comme la Fondation Bill et Melinda Gates, ont pris le contrôle de l’organisation. »
En mars 2020, Tim Schwab21 a souligné les risques moraux de la Fondation Gates qui a donné des centaines de millions de dollars à des sociétés dont elle détient des actions ou des obligations, dont Merck, Sanofi, Lily, Pfizer, Novartis, Teva qui font de plus partie des plus grandes entreprises du monde, telles que GlaxoSmithKline qui développent de nouveaux vaccins et médicaments.
Lionel Astruc estime :
« Une telle participation financière devrait être soumise à un droit de regard des États et des citoyens, tant son pouvoir est grand et sa menace lourde sur nos démocraties »22.
Lors d’une interview au Spiegel23 l’épidémiologiste Tom Jefferson, démontrait les conséquences de la privatisation de l’OMS lors de la crise de la grippe H1N1 :
« Une des caractéristiques les plus ahurissantes de cette grippe, et de tout le roman-feuilleton qui en a découlé, est que, année après année, des gens émettent des prévisions de plus en plus pessimistes. Jusqu’à présent, aucune ne s’est jamais réalisée et ces personnes sont toujours là, à répéter leurs prédictions. Par exemple, qu’est-il arrivé avec la grippe aviaire qui était censée tous nous tuer ? Rien. Mais, ce n’est pas cela qui arrête ces gens de faire leurs prédictions. Parfois, on a le sentiment que c’est toute une industrie qui se prête à espérer une pandémie… L’OMS et les responsables de la santé publique, les virologistes et les laboratoires pharmaceutiques ont construit tout un système autour de l’imminence de la pandémie. Beaucoup d’argent est en jeu, ainsi que des réseaux d’influence, des carrières et des institutions tout entières ! Et il a suffi qu’un des virus de la grippe mute pour voir toute la machine se mettre en branle… « Ne trouvez-vous pas frappant que l’OMS ait modifié sa définition de la pandémie ? L’ancienne définition parlait d’un virus nouveau, à propagation rapide, pour lequel l’immunité n’existe pas, et qui entraîne un taux élevé de malades et de décès. Aujourd’hui, ces deux derniers points sur les taux d’infection ont été supprimés, et c’est ainsi que la grippe A est entrée dans la catégorie des pandémies ».
Lors de la crise H1N1, l’OMS et les gouvernements n’avaient pas réussi à convaincre les populations de la réalité du danger et de l’utilité des vaccins, car les médecins étaient septiques et les médias partagés. Leurs bénéfices des milliardaires ont été moindres qu’espérés, mais ils en ont tiré les enseignements. Lors du Covid, ils contrôlaient totalement l’information officielle et ont disqualifié et/ou interdit les médecins prudents qui s’exprimaient.
L’argent est une drogue très addictive et les super riches en veulent toujours plus. Ils poussent l’OMS à s’arroger encore plus de pouvoir pour asservir davantage et mieux bâillonner les populations lors de la prochaine prétendue épidémie. C’est le but réel des modifications que l’OMS veut apporter au traité sanitaire international (RIS).
Les propositions totalitaires mondiales de l’OMS24 25 26
Le neuvième cycle de négociations sur l’accord mondial de prévention contre les pandémies a commencé le 25 mars 2024. Le directeur de l’OMS Tedros Adhanom Ghebreyesus a présenté son projet de Traité contre les Pandémies et un nouveau règlement sanitaire international prévoyant des transferts majeurs de souveraineté des pays membres vers l’OMS afin de lui permettre de décider d’une politique sanitaire mondiale contraignante à appliquer partout.
1°) Ce projet veut rendre obligatoires les décisions de l’OMS qui jusque-là n’étaient que des recommandations non contraignantes.
2°) Son article 4 veut limiter la souveraineté des états en stipulant « le droit souverain des États n’existe que dans la mesure où les activités des États ne nuisent pas à leurs populations, ni aux autres pays ».
3°) Son article 15 confierait au Directeur général le pouvoir exorbitant de décider seul s’il y a une urgence sanitaire et de son ampleur avec une vaste extension des éventualités pour justifier une urgence, incluant non plus seulement les pandémies, mais aussi le changement climatique, la perte de diversité…
4°) L’article 18 du règlement sanitaire international (RSI) permettrait à l’OMS :
- – d’exiger des examens médicaux ou une vaccination ou toute autre mesure prophylactique, et d’en rechercher les preuves ;
- – de placer en quarantaine les personnes suspectes ou leur appliquer d’autres mesures sanitaires, d’isoler ou de traiter les personnes affectées ;
- – de rechercher les contacts des personnes suspectes ou affectées ou de les soumettre à un dépistage.
Ces propositions supprimeraient en pratique le consentement libre et éclairé des citoyens aux soins et la liberté de prescription des médecins
5°) Les articles 1 et 2 du traité évoquent les « produits de santé » sur lesquels l’OMS aura une autorité totale de se substituer aux agences sanitaires nationales en s’arrogeant :
- – Le droit de choisir les produits de santé, alors même que plusieurs contributeurs de l’OMS sont très liés à l’industrie pharmaceutique.
- – De dresser et publier une liste des produits de santé nécessaires. D’établir et publier des spécifications pour la production des produits de santé nécessaires.
- – D’élaborer des lignes directrices adéquates à l’intention des autorités de réglementation pour l’homologation rapide des produits de santé (…).
- – De créer une base de données sur les matières premières et les fournisseurs éventuels.
- – De créer une bibliothèque des lignées cellulaires pour accélérer la production et l’homologation des produits biothérapeutiques similaires et des vaccins.
- – De passer en revue et mettre à jour la liste des autorités afin de faciliter les homologations qu’elle jugerait utiles.
6°) L’article 44 et l’article 18 du règlement sanitaire international institueraient une censure mondiale pire que celle qu’on a subie depuis le Covid.
En vue de « contrer la diffusion d’informations erronées ou non fiables » et « combattre les informations fausses et trompeuses ou la désinformation ». La définition des informations « fausses et trompeuses ») serait celle de l’OMS :
« [des informations] qui font “obstacle à l’adhésion aux mesures sociales (…) et qui sapent la confiance envers la science et les institutions de santé publique”. »
L’OMS veut ainsi s’ériger ainsi en juge de la vérité scientifique, grand prête du crédo officiel, pouvant décréter hérétique et censurer toute opinion qui serait contraire aux intérêts de ses financeurs, comme l’a fait d’ailleurs fait en France le gouvernement Macron avec son « conseil scientifique Covid » dont les délibérations sont toujours protégées par le secret défense.
Contre l’OMS, réaffirmons partout nos droits fondamentaux !
Lors d’une conférence de presse à Genève le 28 mai 2023, l’Alliance internationale pour la justice et la démocratie a alerté :
« La centralisation du pouvoir dans les mains de l’OMS menace la démocratie ».
Le président Macron, Ursula von der Leyen et le gouvernement américain actuel sont favorables à ces textes liberticides qui vont être reproposés au vote le 26 mai 2024. S’ils étaient acceptés, nous n’aurions plus de recours légaux.
Si nous voulons refuser que notre santé et nos libertés fondamentales dépendent du bon vouloir de l’OMS, des entreprises privées et des milliardaires qui la financent et qui l’inspirent, c’est maintenant que nous devons nous battre !
Les menaces que ce projet de traité font peser sur nos libertés paraissent autrement plus importantes que la discrimination capillaire qui a récemment occupé nos parlementaires ! Exigeons que l’Assemblée Nationale en débatte, que le Sénat crée une commission d’enquête et/ou que la décision soit soumise à référendum.
Nous ne sommes pas seuls à nous battre pour défendre les libertés fondamentales des citoyens : le Syndicat Liberté Santé27, Bon sens,le Collectif des 300, des juristes français et l’International Association of Lawyers for Human Rightset bien d’autres au travers le monde se sont déjà mobilisés.
De nombreux pays ont d’ailleurs déjà refusé de donner leur accord aux propositions autoritaires de l’OMS : dont plusieurs nations africaines avec l’Ouganda comme tête de file, mais aussi l’Iran, la Malaisie, l’Estonie, les Philippines et le Brésil28.
Le ministre britannique adjoint aux Affaires étrangères, Andrew Mitchell, a déclaré au Telegraph « qu’il bloquerait toute loi empêchant le Royaume-Uni d’établir sa propre politique de santé ».
Le Sénat de l’État de Louisiane a adopté à l’unanimité le projet de loi 133, une déclaration claire de souveraineté contre l’agenda de l’ONU, de l’OMS et du FEM.
« Aucune règle, réglementation, frais, taxe, politique ou mandat de quelque nature que ce soit de l’Organisation mondiale de la santé, des Nations Unies et du Forum économique mondial ne sera appliqué ou mis en œuvre par l’État de Louisiane ou par toute agence, département, conseil, commission, subdivision politique, entité gouvernementale de l’État, paroisse, municipalité ou toute autre entité politique ».
Informons nos élus pour qu’ils prennent conscience du problème et qu’ils persuadent notre gouvernement d’adopter une attitude semblable. La France ne peut pas abandonner le premier terme de sa devise : LIBERTÉ.
Lire ou écouter aussi :
Appel solennel de N. Farage ex-député européen Nigel Farage plaide pour que tout le monde dise non au Traité sur la pandémie de l’OMS :
« Il s’agit littéralement d’un traité mondialiste qui enlève le pouvoir à l’État-nation. Nous ne devrions pas verser d’argent à cette épouvantable organisation. »
« Là où le Professeur Perronne pourrait aller plus loin, c’est que c’est vrai pour l’environnement, pour les antibiotiques, c’est vrai pour tout !»
@DIVIZIO1
alerte sur l’élargissement considérable du champ d’action de l’OMS dans le cadre de son action #OneHealth. De la…
Et bien d’autres. Le combat est international. Poursuivons-le et nous le gagnerons !



 VDT Déclin A3 Sophie L 2023 Copier 02 (youtube.com)
VDT Déclin A3 Sophie L 2023 Copier 02 (youtube.com)