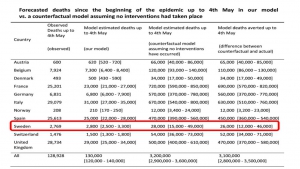
Bilan chiffré des confinements en France et à l’international : une catastrophe sanitaire générale
Par le dr G Delépine
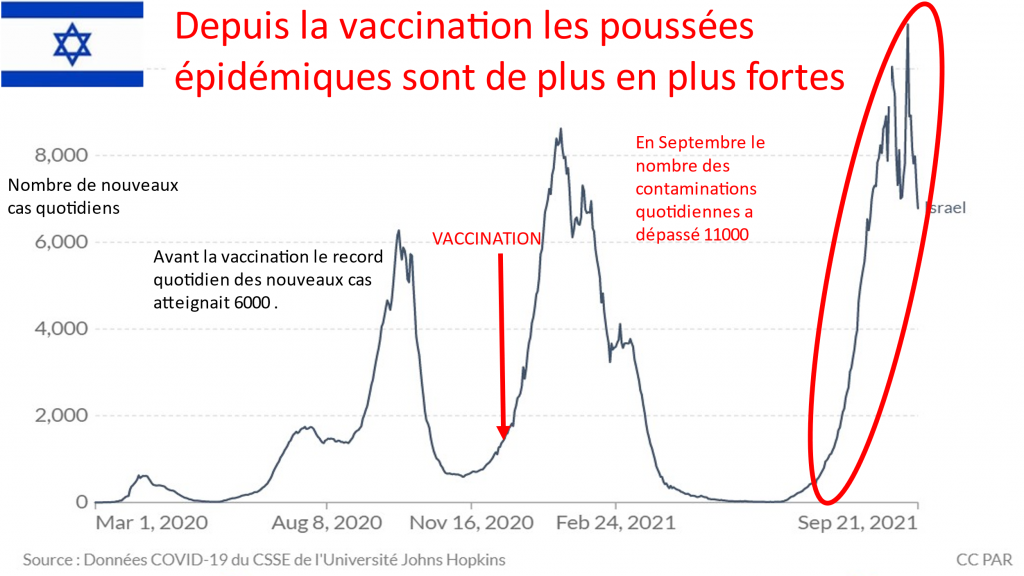
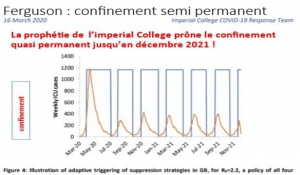
Depuis le début de la crise, le gouvernement impose des mesures contre-productives en santé, aggravant la misère des plus pauvres et ruinant les classes moyennes et les petits commerçants pour faire accepter des médicaments hors de prix et dangereux, des vaccins bâclés et des lois de régression sociale. Il suit en cela fidèlement les prescriptions du conseil sanitaire de l’OMS et de son faux prophète Ferguson[1] qui a d’emblée affirmé qu’il faudrait confiner au moins jusqu’en décembre 2021, ou l’arrivée d’un traitement miracle[2], ou les vaccins sans se préoccuper des conséquences catastrophiques de ses préconisations.
Ceci s’intègre dans le cadre de l’agenda du forum de Davos décidé par l’oligarchie mondialiste dans les mains des milliardaires mondiaux en accord avec les gouvernements liés et actuellement réunis en forum virtuel.
Ce bilan sanitaire est d’autant plus d’actualité que le conseil prétendument scientifique composé de médecins trop proches de l’industrie appellent sur tous les médias à un troisième confinement sans aucune justification médicale, pour raviver le chantage « vous serez astreint à domicile à vie ou vacciné ! »
Dans ce chapitre, nous dresserons le bilan sanitaire des mesures liberticides qui nous ont été imposées. Pour rester le plus factuel possible cette analyse repose principalement sur les données publiées par l’OMS, les agences sanitaires des pays concernés et les organismes internationaux comme l’OCDE, illustrés par des interviews de médecins de terrain.
Effets constatés du confinement sur la propagation de l’épidémie
Une étude de l’OCDE sur les confinements de la première vague précise que sur les 31 pays européens étudiés, la moitié (16) ont demandé à leurs citoyens de rester chez eux durant la première vague. Ces confinements plus ou moins souples et plus ou moins obligatoires ont duré 47,5 jours en moyenne. Cinq grands pays ont basé leur politique sanitaire sur le confinement aveugle (sans isoler les malades des autres) de toute leur population : l’Italie, l’Espagne, la Belgique, la France et la Grande-Bretagne. Les plus durs ont été la France et l’Italie avec 55 jours, l’Espagne avec 50 jours et le Royaume-Uni avec 46 jours.
A l’opposé les Pays-Bas, la Suède, la Finlande, la Biélorussie ont fait confiance à leurs citoyens en leurs prodiguant des conseils et en les laissant libres de circuler.
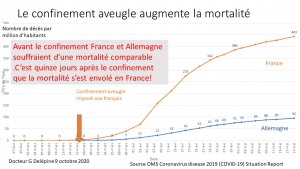
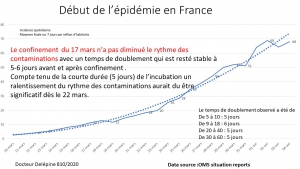
L’étude des courbes de progression de la maladie dans les différents pays d’Europe par la recherche des inversions de tendance (break point analysis)[3] montre que le confinement aveugle a été incapable de ralentir la progression de l’épidémie.
En France, le nombre des contaminations n’a diminué qu’en avril, six semaines après le début de l’épidémie, en même temps qu’aux Pays-Bas et en Allemagne, pays qui n’ont pas astreint à domicile leurs populations.
Cette régression spontanée après 6 semaines d’évolution paraît une caractéristique de cette maladie d’après le professeur Ben Israel[4] « C’est comme ça partout dans le monde. Tant dans les pays où ont été prises des mesures de confinement comme l’Italie, que dans les pays qui n’ont pas eu de confinement comme Taiwan ou Singapour. Dans tel ou tel pays, il y a une augmentation jusqu’à la quatrième ou la sixième semaine, et immédiatement après la régression jusqu’à ce qu’elle disparaisse au cours de la huitième semaine.”
Les autorités norvégiennes ont reconnu l’inutilité du confinement
La Norvège est fréquemment citée comme preuve de l’efficacité du confinement par ses partisans français, mais ce n’est pas l’avis de l’autorité sanitaire norvégienne qui a publié un rapport dont la conclusion est sans ambiguïté : le virus était déjà en voie de disparition lorsque le verrouillage a été ordonné. Camilla Stoltenberg, directrice générale de l’Institut norvégien de santé publique précise ainsi [5] « le confinement n’était pas nécessaire pour gérer le covid-19 car le taux de reproduction effectif était déjà tombé à environ 1,1 lorsque les mesures les plus restrictives ont été mises en œuvre le 12 mars ».
Impact des confinements à l’international : échec général
De nombreuses autres études [6] [7] [8] [9] [10] [11] [12] ont évalué l’effet des mesures coercitives sur les évolutions constatées de l’épidémie. Aucune n’a montré qu’elles auraient pu avoir un impact positif sur l’épidémie. C’est le cas de l’étude danoise sur le Nord Jutland [13] de l’étude néo- zélandaise[14], de l’analyse indienne[15], de l’étude des pays d’Europe occidentale[16] et de toutes les études internationales basées sur les faits avérés. Les seuls articles prétendant qu’il existerait un avantage au confinement sont celles qui n’analysent pas les faits constatés, mais reposent sur des simulations et des scénarios sans rapport avec la réalité.
Pour innocenter les gouvernements qui ont astreint leur population à domicile, on pourrait croire que les pays qui ont confiné policièrement l’ont fait parce que leur situation était plus menaçante au moment où ils en ont pris la décision.
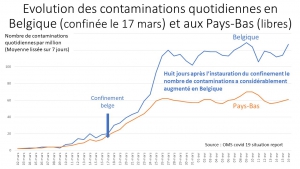
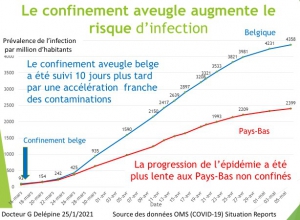
Mais la comparaison des contaminations en Belgique et aux Pays-Bas (pays les plus proches par leurs origines ethniques, leur mode de vie et l’âge moyen de leurs habitants) montre qu’il n’en est rien; avant le confinement belge, le nombre quotidien des contaminations par million d’habitants évoluait de la même manière dans ces deux pays frères; ce n’est que dix jours après le début du confinement belge que le nombre de malades a fortement augmenté en Belgique tandis qu’il progressait sans modification aux Pays-Bas.
Les raisons de l’augmentation des contaminations par le confinement aveugle sont simples ; le traitement traditionnel des épidémies (l’endiguement-quarantaine) repose sur la séparation des malades des sujets sains ; le confinement aveugle prévoit au contraire de renvoyer les malades sans signes de gravité dans leur famille, et les pensionnaires d ’Ehpad dans leur établissement d’origine favorisant ainsi la contamination de leur entourage.
L’étude récente Comcor[17] sur les lieux de contamination rapporte que le tiers d’entre eux est le foyer familial où l’un des parents a contaminé l’autre ou son/ses enfants confirme cette hypothèse.
Le confinement aveugle entraîne une augmentation de la mortalité liée au Covid19.
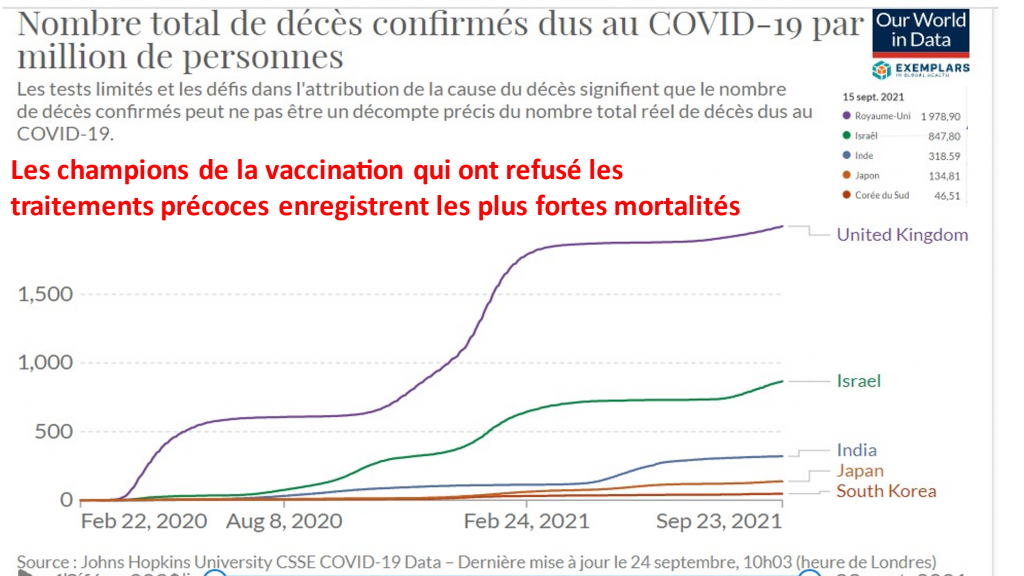
Les données de l’OMS du 26 janvier 2021[18] prouvent que le confinement aveugle est contre-productif : les pays qui ont confiné policièrement sans isoler réellement les malades sont tous dans le top 5 européen des plus fortes mortalités globales attribuées au Covid19
avec respectivement : Belgique : 1793/Million, Italie : 1245/M, Espagne : 1177/M, Grande-Bretagne : 1443/M, France : 1113/M
contre 790/M pour les Pays-Bas, 117/M en Finlande, 173/M en Biélorussie et 1090/M en Suède. La probabilité qu’une telle distribution des mortalités selon les mesures sanitaires soit due au seul hasard n’est que 0,007[19].
Ferguson et ses élèves se glorifient de leurs erreurs de prédictions.
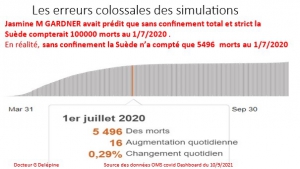
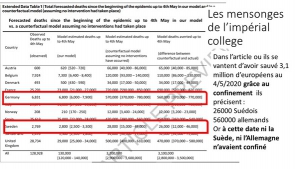
De nombreux articles d’auteurs proches de Ferguson ou des responsables du confinement aveugle prétendent qu’il aurait sauvé des vies ; il ne s’agit que de propagande totalement mensongère qui repose sur la comparaison entre leurs prévisions très exagérées de mortalité et les mortalités réellement observées à une date donnée. Ainsi, plus ils se trompent par excès dans leurs estimations initiales et plus ils se gargarisent ultérieurement des morts virtuelles évitées. Dans un article de Nature, ils prétendent ainsi avoir sauvé 3 millions d’européens et en particulier 26000 suédois, grâce au confinement, sans avoir remarqué que les suédois n’avaient jamais confiné et que leur chiffre de 2800 morts recensés au 5 mai prouvait seulement que leur prévision surestimait par dix le risque réel.
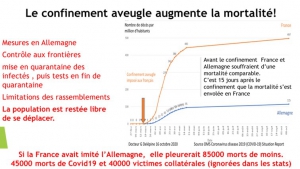
De même pour l’Allemagne ; le rapport 9 de l’Impérial College affirmait que la technique classique d’endiguement ne pourrait pas ralentir l’épidémie et que si l’Allemagne ne confinait pas elle pleurerait 570000 morts au 5 mai 2020. L’Allemagne n’a pas confiné à l’aveugle mais simplement pratiqué l’endiguement et ne comptait au 5 mai que 6800 décès attribués au Covid19. Mais l’équipe de Ferguson prétend que 560000 allemands auraient été sauvés grâce au confinement (qui n’a pas été pratiqué) !
Lancetgate et Naturegate
Dans le scandale du Lancet Gate, les auteurs avaient inventé des données pour affirmer que la chloroquine était dangereuse. Dans ce qui peut s’appeler le Nature Gate, il n’y a pas eu fabrication de données mais refus de regarder la réalité des mesures réellement utilisées pour se glorifier de ses erreurs ; il est étonnant qu’aucun membre du comité de lecture d’une revue de bonne réputation ne se soit rendu compte des erreurs de raisonnement et des mensonges sur les politiques suédoises, néerlandaises et allemandes aboutissant à une aussi grosse supercherie.
La même technique de glorification frauduleuse du confinement par des simulations a été utilisée en France par 3 élèves de l’école supérieure de santé publique prétendant[20] que le confinement aurait sauvé 60000 français. Leurs conclusions, non validées par des pairs, ont été immédiatement présentées aux députés par le premier ministre comme justification du confinement. Les erreurs de conception, des hypothèses et des conclusions d’un étude vraisemblablement commandée par le pouvoir ont été depuis largement démontrées dans des revues scientifiques[21] [22] [23] mais les médias mainstream en ont très peu parlé[24].

Le confinement a créé des victimes d’autres pathologies (victimes collatérales)
En France, quelques jours avant le premier confinement, les Agences Régionales de Santé ont activé le plan blanc réservant tous les moyens sanitaires publics et privés aux malades du Covid19 et interdisant entre autres aux chirurgiens d’opérer sauf les extrêmes urgences vitales, en négligeant les malades ordinaires. Elles ont ainsi laissé des pans entiers de nos hôpitaux vides, tant dans le public que le privé et conduit à la mise au chômage partiel de nombreux personnels de soins, infirmières, aide- soignants, ambulanciers, manipulateurs radios empêchés de traiter les malades ordinaires.
Les traitements médicaux sont d’autant plus efficaces qu’utilisés tôt et bien surveillés. Leur absence, leur retard ou leur mauvaise surveillance ont des conséquences critiques sur la vie des malades, sans compter l’angoisse générée et leur effet connu sur la diminution des défenses immunitaires. La notion de traitement « précoce » doit s’évaluer avec le médecin traitant dont on tente de plus en plus à minimiser le rôle pourtant essentiel pour l’adaptation des soins à chaque personne unique.
On peut estimer à 40 000 victimes supplémentaires actuelles et/ou futures par les défauts de soins et regretter le silence de la plupart des politiques et des médias pour ces victimes.
Malades urgents d’autres pathologies, déjà morts des confinements
En Ile-de-France, la crise a fait chuter les consultations de 40 % chez les généralistes, de près de 70 % chez les spécialistes et l’activité des urgences a fortement régressé. « Les Franciliens ont eu moins recours aux soins, ce qui peut malheureusement engendrer, pour les cas les plus graves, des décès. » a avoué l’agence régionale de santé d’Ile-de-France
Le professeur Johanne Silvain, chirurgien cardiaque à la Pitié- Salpêtrière a précisé que trois quarts des opérations programmées ont été reportées. « Quand on a rappelé des patients pour fixer de nouvelles dates, certains étaient décédés entre-temps ».
Mais comme prétend encore le ministre et comme le répètent toujours en boucle les médias « le confinement permet de sauver des vies » …
Le Monde rapporte le cas d’une Parisienne de 65 ans qui a subi un gros infarctus à son domicile, mais a préféré rester confinée. Sept jours plus tard, elle est conduite à la Pitié-Salpêtrière. Elle meurt d’une « rupture cardiaque ».
Une étude de l’Inserm menée par le chercheur Eloi Marijon au Centre de Recherche Cardiovasculaire de Paris (Inserm/Université de Paris) en collaboration avec Daniel Jost (Brigade des sapeurs-pompiers de Paris) montre que pendant la période du confinement, le nombre d’arrêts cardiaques en région parisienne a été multiplié par deux par rapport à la même période les années précédentes et que leur taux de guérison a été divisé par deux.
En Grande-Bretagne, une étude portant sur neuf hôpitaux a constaté que durant le confinement le nombre total d’admissions et de fréquentation aux urgences a diminué de 57,9% par rapport à l’année précédente. L’activité pour les affections cardiaques, cérébro-vasculaires et autres affections vasculaires a chuté de 31% à 88% après le verrouillage, avec les plus fortes réductions observées pour les pontages coronariens, l’endartériectomie carotidienne, la réparation de l’anévrisme de l’aorte et la maladie artérielle périphérique.
Les chances de guérison des accidents vasculaires cérébraux (AVC) dépendent considérablement de l’extrême précocité de leur traitement. Mais le docteur F Rouanet, de l’hôpital Pellegrin à Bordeaux a vu, pendant vingt jours, le nombre de diagnostics d’AVC baisser de 50 %. « On ne sait pas ce qu’ils sont devenus. La pathologie, elle, n’a pourtant pas disparu, cela nous fait craindre une hausse brutale des accidents et de la mortalité. »
Pourquoi les prévisions de Ferguson et les décisions des gouvernements obéissants n’ont-elles pas prévu ces morts indirectes bien réelles pour ne s’intéresser qu’aux morts Covid virtuelles imaginés par des simulations mathématiques fausses ?
Malades chroniques abandonnés à cause du plan blanc
En France, 20 millions de personnes souffriraient de pathologies chroniques, prises en charge à 100 % par la sécurité sociale. Chaque année, plus de 600 000 d’entre elles nécessitent des soins réguliers, près de 320 000 des chimiothérapies, 210 000 des séances de radiothérapie, et plus de 82 000 doivent être dialysés trois fois par semaine pour insuffisance rénale. La télémédecine tant vantée par les énarques désincarnés ne peut remplacer le contact humain direct avec le malade. Des patients fragiles, angoissés, désespérés, dont les retards de consultations et de traitement ont accru les complications et la mortalité.
Les traitements des cancéreux ont été désorganisés par les injonctions des ARS[25]. Des cures de chimiothérapie ont été espacées ou modifiées, remplaçant un traitement par voie intraveineuse par un traitement oral, éventuellement moins efficace pour s’adapter au blocage des lits d’hospitalisation. Des opérations urgentes ont été annulées, remises à période ultérieure sans précision sur une éventuelle reconvocation. C’est l’ARS qui a bloqué les opérations, les décrétant non urgentes et possiblement remplacées par de la chimiothérapie et/ou de la radiothérapie ! Raisonnement médical perdu, médecins transformés en robots devant obéir à des administratifs sous la surveillance inquisitoriale des agences régionales de santé, petites dictatures locales contre lesquelles il n’existe aucune voie de recours. Il semble bien que cela a recommencé lors des autres confinements puisque le préfet d’ile de France a décrété depuis mi-septembre le plan blanc alors que le nombre de morts attribués au Covid est très inférieur à celui de mars.
Cette rupture de soins ne concerne pas uniquement la cancérologie, mais a touché toutes les pathologies : cardiologie, neurologie, endocrinologie, rhumatologie, insuffisance rénale (la moitié des greffes rénales programmées n’ont pas été réalisées) etc.
Compte tenu du nombre considérable de malades chroniques et de leur poids dans la mortalité globale, ce sont plusieurs dizaines de milliers de décès prématurés évitables que ces arrêt/modifications de soins ont/vont entraîner. Impossible de prévoir précisément leur nombre car évidemment cela va se compter sur des années.
Malades nouveaux diagnostiqués et traités avec retard
Dans tous les pays, la baisse considérable des consultations a entrainé des retards diagnostiques très inquiétants : même si leurs conséquences à venir sont pour l’instant difficiles à mesurer avec précision.
En cardiologie, au Danemark une baisse de 47% des nouveaux cas de fibrillation auriculaire a été observée. De même, le nombre de patients hospitalisés avec une aggravation de l’insuffisance cardiaque ou un diagnostic de nouvelle apparition a été nettement réduit après le confinement soulevant « des inquiétudes quant à un sous-traitement potentiel de l’IC actuellement qui pourrait avoir un impact sur le pronostic à long terme ».
Le drame des cancéreux
En cancérologie en France, 380.000 nouveaux cas de cancer sont détectés chaque année, soit environ 30.000 par mois. Durant le premier plan blanc[26] 75.000 nouveaux cancers auraient dû être diagnostiqués si les chirurgiens avaient pu opérer.
L’académie de chirurgie s’en est inquiétée (assez tard) dans son communiqué du 15 Mai 2020 : « depuis la mise en place du Plan Blanc le 13 mars, 85% des 7,2 millions d’interventions chirurgicales programmées chaque année en France ont été reportées, soit près d’1,1million d’actes (CNAMTS, ATIH). Il en résulte des risques d’aggravation dus au retard de prise en charge, non seulement en oncologie, mais également dans les autres disciplines ».
Durant le confinement, ce chiffre semble être descendu de moitié. En cancérologie l’Institut Curie a vu le nombre des urgences et consultations pédiatriques reculer de 30 %. Les adultes sont aussi concernés par ces retards de diagnostic, notamment pour les formes de cancer les plus agressives, comme celui du poumon. Le professeur F. Le Tourteau du département de l’oncologie médicale de Curie témoigne : « pendant trois semaines, au lieu de 15 à 20 personnes par jour aux urgences, on n’avait que 2 à 3 patients et on s’attend à une vague de diagnostics à des stades plus graves ».
Un constat partagé par l’institut Gustave-Roussy où « les urgences ont perdu 50 % de leur fréquentation. On a envoyé des messages d’information aux 15 000 personnes inscrites dans nos fichiers, on a eu moins de 10 % de réponses ».
Les auteurs de l’étude estiment à près de 10000 morts les conséquences prévisibles des retards de diagnostic pour les seuls cancers du sein et du colon.
Les dermatologues espagnols ont constaté : « en l’absence de diagnostic et de traitement adéquats du carcinome et du mélanome, la survie spécifique à la maladie à 2, 5 et 10 ans chez les patients dont la chirurgie a été retardée de 3 mois a diminué de 6,2%, 8,2% et 5,2%, respectivement ».
Au Royaume-Uni, the Centers for Disease Control and Prevention estiment que, « du fait du confinement, une augmentation de mortalité de 20% des nouveaux cancers est à craindre. »
Une autre étude britannique estime à 59 204 – 63 229 ans le nombre d’années de vie perdues pour les seuls cancers colo-rectaux, du sein, de l’œsophage et du poumon en raison des retards de diagnostic dus au confinement.
En France « nous craignons 5.000 à 10.000 morts supplémentaires du cancer”, explique Jean-Yves Blay, du centre d’oncologie Léon Bérard de Lyon. « Ces estimations sont même plutôt optimistes, les anglais ont des projections allant jusqu’à 40.000 patients décédés en excès.”
Si on fait la somme des morts en excès toutes pathologies or Covid confondues, le bilan mortifère des retards diagnostiques s’élève actuellement pour la France à plus de 40000 morts à venir. Cette estimation ne constitue qu’un minima
L’hécatombe programmée de nos ainés
Le confinement avait pour premier prétexte de protéger particulièrement nos ainés, mais dix mois de mesure sanitaires inventées de toutes pièces sans fondement scientifiques ont abouti à une hécatombe sans précédent.
Pour les vieillards, pensionnaires des EHPAD, la solitude complète imposée par le confinement les a conduits au « syndrome de glissement » et à la mort, presque aussi sûrement que le virus. Quelle ineptie et quelle honte de leur interdire les visites de leurs proches, alors que leurs soignants sortent chaque jour et prennent des transports publics bondés et reviennent un jour ou l’autre porteurs du virus qu’ils propagent à leur insu car scandaleusement peu protégés. Et que dire de l’interruption des rééducations en particulier pour dysphagie nécessaires à beaucoup des pensionnaires ?
Et que penser de la note du ministère aux directeurs d’EHPAD précisant clairement que les personnes âgées malades ou susceptibles de l’être ne doivent en aucun cas être adressées aux urgences, car elles ne seront ni hospitalisées, ni traitées, ni réanimées. Précisons qu’il s’agit de critères d’âge, sans tenir aucun compte de l’état physique et intellectuel des résidents. Nous connaissons tous de beaux vieillards de plus de 90 ans et des « très vieux » de 70 ans ou moins. Les médecins ont toujours pesé ces éléments du temps où ils pouvaient exercer leur vocation selon Hippocrate, et non sous l’autorité dictatoriale de bureaucrates interdisant d’hospitaliser les infectés de plus de 70-75 ans « afin qu’ils ne puissent pas occuper inutilement les lits de réanimation ». Les nazis à la descente du train de déportés triaient selon l’âge physiologique. Pas nos bureaucrates. Les plus de 70 ans infectés sont renvoyés dans leurs EHPAD ou faute de possibilité d’isolement réel, de traitement, de personnel et de matériel de protection, ils contaminent leurs compagnons d’infortune sans même pouvoir dire adieu à leurs familles. Et pour tout traitement le ministre propose le Rivotril censé leur adoucir la mort. Nos technocrates auraient-ils imaginé un début de solution au financement des retraites par le génocide des plus vieux retraités, suivant ainsi les conseils de J. Attali, mentor du président ?
Les récits dramatiques se succèdent sur les réseaux sociaux. Couples déchirés dans leurs derniers moments, enfants qui ne reverront jamais leur mère, soignants qui veillent depuis des mois ou années sur des vieillards et les voient brutalement contaminés, refusés d’hôpital, interdits de réanimation, privés de traitement, abandonnés à la mort sans personne pour leur tenir la main puis jetés au tombeau en catimini, sans accompagnement, les familles recevant des contraventions s’ils se retrouvent pour les accompagner au cimetière. Avec l’épidémie de décès dans les EHPADs, les proches risquent même la prison pour récidive d’infraction (présence aux enterrements), en attendant peut-être qu’on les condamne à mort comme l’Antigone de Sophocle, emmurée vivante pour avoir bravé l’interdiction royale d’enterrer son frère. Eternel combat de la morale qui définit notre humanité contre des lois tyranniques injustifiés.
Les victimes de pathologies psychiatriques
Le nombre de victimes de maladies organiques du confinement doit être complété par les conséquences des confinements sur les pathologies psychiatriques en traitement, les nouveaux malades psychiques, et les futurs suicides liés entre autres à la crise économique.
Les complications psychiques des personnes saines confinées sont nombreuses et bien connues : dépressions qui persistent dans plus d’un tiers des cas de nombreux mois après sa levée, stress post-traumatique durable, obésité, drames familiaux, divorces, retard scolaire, addiction renforcée à l’alcool aux drogues ou aux écrans. Les complications médicales et sociales de cette mesure moyenâgeuse inefficace, sont avérées et souvent catastrophiques.
Tous les confinés interrogés décrivent un sentiment d’isolement et le manque de contacts sociaux. L’absence de tout contact physique avec les membres de la famille et amis confinés ailleurs, est particulièrement mal vécu surtout lorsque le confinement aveugle est prolongé.
Certains groupes de personnes sont encore plus à risques. Enfants placés, qui se retrouvent encore plus seuls avec la moitié des encadrants absents. Femmes et/ou enfants victimes de violence familiales confinées avec leurs bourreaux eux-mêmes agacés par l’absence de sortie et paniqués par le Covid19. Prisonniers et malades des hôpitaux psychiatriques privés de visites facilitants le syndrome de glissement.
Mais plus généralement les enfants ainsi que le rappellent[27] des professionnels en psychologie, psychanalyse, pédiatrie et pédopsychiatrie qui : « relèvent de graves perturbations dans le vivre-ensemble et la socialisation, la survenue de nouvelles maltraitances au sein des établissements, une condamnation de la tendresse, de l’empathie et un interdit implicite à l’altérité, une entrave au développement relationnel, psychomoteur ainsi que des régressions dans les apprentissages, une fragilisation majeure de l’autorité bienveillante/contenante et de la posture parentale, une perte de repères structurants et des discours paradoxaux. Le tableau clinique conclut à une souffrance psychique croissante chez les enfants, risquant d’entraîner une explosion de troubles psychiques graves et de passages à l’acte suicidaires. »
Les adolescents privés de leurs premières amours sont complètement déprimés, le téléphone et même Skype et/ou face time, Instagram ou WhatsApp ne pouvant en rien remplacer l’intimité qu’ils commençaient à découvrir. Même leur école et leurs professeurs en chair et en os qu’ils critiquaient souvent leur manquent cruellement. Les adolescents sportifs de haut niveau sont particulièrement menacés car ils ont été privés des entraînements et des compétitions nationales permettant de sélectionner nos futurs champions afin de mieux les préparer aux épreuves internationales proches.
Accouchées et nouveaux nés privées de la visite de leurs proches dans une période pourtant anxiogène pour ces jeunes femmes particulièrement en période de psychose publique organisée.
L’aggravation de la famine par les confinements tue les enfants
Le Covid19 ne tue pas les enfants, mais la famine consécutive aux confinements les menace directement[28].
La famine est déjà réapparue en France[29] [30]. Le secours populaire, le secours catholique et les restos du cœur sont débordés, et on lit de plus en plus de témoignages de mamans : « j’ai inscrit ma fille à la cantine et ne mange plus le midi, non par gout mais par économie. On s’habitue… »
C’est aussi le cas en Italie[31] où les enfants affamés italiens à la suite de la politique italienne délétère à l’origine d’un nombre de morts directs des plus élevés mais également de morts indirectes très élevées.
Dans les pays pauvres, d’après les responsables de l’ONU[32], de l’Oxcam[33] et du programme alimentaire mondial contre la faim[34], l’aggravation de la famine risque d’entraîner plus d’une centaine de millions de morts.
Les principales fautes de notre politique sanitaire
Le comité prétendument scientifique et notre premier ministre suivent l’exemple de Ferguson et ses élèves et continuent de se glorifier de leur politique sanitaire malgré les résultats catastrophique sur la mortalité attribuée au Covid19. Ce déni permanent de la réalité est très inquiétant pour l’avenir car comme le disait A. Einstein : « ce n’est pas avec ceux qui ont créé les problèmes qu’il faut espérer les résoudre ». Rappelons la liste de leurs autres principales erreurs :
-Ils ont cru un mathématicien-prophète prônant le confinement aveugle sans évaluer ses conséquences au lieu d’utiliser la technique médicale éprouvée d’endiguement-quarantaine.
-Ils ont créé un comité prétendument scientifique en réunissant les personnes les plus liées aux firmes pharmaceutiques dont peu de cliniciens, et lui ont accordé un pouvoir discrétionnaire sur nos libertés.
-Ils ont interdit aux médecins de ville de traiter les malades comme ils le jugeait utile : interdiction de la chloroquine, puis interdiction de l’azithromycine et même de l’ivermectine récemment.
-Ils ont interdit l’admission des vieillards en réanimation, puis à l’hôpital puis aux urgences pour les renvoyer sans traitement dans leurs Ephads d’origine
-Ils ont conseillé d’euthanasier par Rivotril sans leur consentement les vieux simplement suspects de Covid19 (les tests leur étant refusés)
-Ils ont discrédité les médecins opposés à leurs mesures infondées, rétabli le délit d’opinion pour les médecins par un décret du 22 décembre 2020, et font poursuivre par le conseil de l’ordre les donneurs d’alerte.
Pourquoi devrions-nous attendre la fin de l’épidémie pour réagir ?
C’est maintenant que nous devons nous soulever pour stopper cette monstruosité, ce génocide de nos ainés qui se poursuit dans les EHPADs, et de nos jeunes isolés, privés de ce qui fait le sel de la vie, les contacts avec les autres humains.
Que chacun d’entre nous joigne le maximum d’élus, maires, conseillers régionaux et députés, sénateurs pour qu’ils transmettent au gouvernement la réalité des chiffres, montrant que le confinement aveugle général s’accompagne de beaucoup plus de morts que l’isolement ciblé des malades et de leurs contacts.
Les mesures sanitaires ont tué plus de français qu’elles n’auraient pu en sauver et sont responsables de notre rang de 5ème européen des plus fortes mortalités Covid19. Elles vont en tuer davantage dans les mois et années qui viennent.
Et ils veulent nous reconfiner !
Stop à toutes ces mesures sanitaires sans justification scientifiques. Liberté.
[1] Celui qui avait prédit 70000 morts en Suède et 100000 aux Pays-Bas s’ils ne confinaient pas qui, sans confinement, n’en comptent au 5/1/21 respectivement 8727 et 11612
[2] Mais l’opération « tous pour le Remdesevir » soutenue par les médecins liés à Gilead, le conseil prétendument scientifique et le directeur de l’AP-HP Martin Hirsch a piteusement échouée faisant reporter tous leurs efforts sur la promotion des vaccins
[3] Très utilisée en économie et en cancérologie
[4] Professeur Ben-Israel « Je propose que nous mettions fin aux confinements immédiatement…”
interview à Israel National News 16 avril 2020
[5] Norvège : “le confinement n’était pas nécessaire contre le coronavirus” 29 mai 2020 Strategika
[6] Rabail Chaudhry, George Dranitsaris, Talha Mubashir, Justyna Bartoszko, Sheila Riazi Une analyse au niveau national mesurant l’impact des actions gouvernementales, de la préparation du pays et des facteurs socio-économiques sur la mortalité COVID-19 et les résultats sanitaires associés ». EClinicalMedicine 25 (2020) 100464
[7] Christof Kuhbandner, Stefan Homburg, Harald Walach, Stefan Hockertz. « Le verrouillage de la couronne allemande était-il nécessaire ? » Sage Preprint, 23 juin 2020.
[8]Simon N. Wood. Les infections au COVID-19 ont-elles diminué avant le verrouillage du Royaume-Uni ? Pré-impression de l’Université Cornell, 8 août 2020.
[9]Stefan Homburg et Christof Kuhbandner Commentaire sur Flaxman et al. (2020) : Les effets illusoires des interventions non pharmaceutiques sur le COVID-19 en Europe » par. 17 juin 2020. Advance, Sage Pre-Print
[10] Ben Israel Analyse de la transmission du virus par le professeur. 16 avril 202
[11] Paul Raymond Hunter, Felipe Colon-Gonzalez, Julii Suzanne Brainard, Steve Rushton « Impact des interventions non pharmaceutiques contre le COVID-19 en Europe : une étude quasi expérimentale ». MedRxiv Pre-Print 1er mai 2020
[12] « Lockdown and Closures vs COVID – 19 : COVID Wins » par Surjit S Bhalla, directeur exécutif pour l’Inde du Fonds monétaire international
[13] Kasper Planeta Kepp Christian Bjørnskov Lockdown Effects on Sars-CoV-2 Transmission – The evidence from Northern Jutland https://www.medrxiv.org/content/10.1101/2020.12.28.20248936v1.full.pdf
[14] John Gibson Government mandated lockdowns do not reduce Covid-19 deaths : implications for evaluation the stringent New Zealand response 18 Aug 2020, https://doi.org/10.1080/00779954.2020.1844786 « Les verrouillages imposés par le gouvernement ne réduisent pas le nombre de décès liés au Covid-19 : implications pour l’évaluation de la réponse rigoureuse de la Nouvelle-Zélande »
[15] Surjit S Bhalla Lockdowns and Closures vs COVID – 19 : COVID Wins Nov 1, 2020 http://ssbhalla.org/wp-content/uploads/2020/10/Lockdowns-Closures-vs.-COVID19-Covid-Wins-Nov-4.pdf
[16] Thomas Meunier Full lockdown policies in Western Europe countries have no evident
impacts on the COVID-19 epidemic. https://www.medrxiv.org/content/10.1101/2020.04.24.20078717v1.full.pdf
[17] https://www.pasteur.fr/fr/espace-presse/documents-presse/etude-comcor-lieux-contamination-au-sars-cov-2-ou-francais-s-infectent-ils
[18] https://covid19.who.int/
[19] Calcul direct des probabilités
[20] site internet de l’Ecole des Hautes Etudes de la Santé Publique, sur une page depuis supprimée (https://www.ehesp.fr/2020/04/23/une-etude-inedite-de-chercheurs-de-lehesp-montre-que-le-confinement-aurait-sauve-au-moins-60-000-vies/).
[21] Eric Le Bourg, Quentin de Larochelambert, Jean-François Toussaint Etude critique d’une modélisation des effets du confinement Journal International de médecine 2 mai 2020
[22] Aurélie Haroche Quand les politiques confondent modélisations mathématiques et astrologie, Journal International de Médecine, 25 avril 2020
[23]Gilles Pech de Laclause 1 Arnaud Delenda Lana Augustincic Confinement strict, surcharge hospitalière et surmortalité : Analyse statistique et étude mathématique de l’épidémie de « Covid 19 »
[24] Roland Salmon : https://www.lemonde.fr/idees/article/2020/04/08/roland-salmon-les-donnees-pour-soutenir-la-politique-du-confinement-font-defaut_6035949_3232.html
[25] Agences régionales de santé
[26][26] Interdiction pour les chirurgiens publics ou privés d’opérer les malades non urgents, l’urgence étant décidée par l’ARS et non le chirurgien ou son malade, décret d’Edouard Philippe début mars 2020
[27] https://www.francesoir.fr/opinions-tribunes/impacts-traumatiques-de-la-politique-sanitaire-actuelle-sur-les-enfants-un-constat
[28] France culture La faim plus dangereuse que le coronavirus ? 01/05/2020 https://www.franceculture.fr/emissions/radiographies-du-coronavirus/la-faim-plus-dangereuse-que-le-coronavirus
[29] D’après le canard enchaîné Georges-François Leclerc, préfet de Seine-Saint-Denis aurait écrit : « Je redoute des émeutes de la faim. Nous comptons entre 15.000 et 20.000 personnes qui, entre les bidonvilles, les hébergements d’urgence et les foyers de travailleurs migrants vont avoir du mal à se nourrir ».
[30] « Dans mon frigo, il y a de l’eau, du jus d’orange et deux yaourts », a ainsi témoigné Viviane, habitante de Stains, sur France bleu.
[31] Sara Rosenbaum et AFP Coronavirus en Italie : 700.000 enfants en difficulté alimentaire RTL 10/5/2020 https://www.rtl.fr/actu/international/coronavirus-en-italie-700-000-enfants-en-difficulte-alimentaire-7800498903
[32] » Tiphaine Walton, porte-parole du Programme alimentaire mondial de l’ONU : » Ce qui nous inquiète, c’est la récession économique qui va être engendrée par le coronavirus. On estime qu’il y a plus de personnes qui vont mourir à cause de cette récession qu’à cause du virus en lui-même »
[33] Oxfam, Le nombre de personnes menacées de famine en Afrique de l’Ouest pourrait quasi tripler en trois mois et concerner 50 millions de personnes en août, mardi 21 avril.
[34] Margot van der Velden, directrice du bureau des urgences du PAM :« Lorsque nous déclarons une famine, cela signifie que de nombreuses vies ont déjà été perdues. Si nous attendons d’être sûrs qu’elle soit là, des personnes ont déjà perdu la vie »,